이종금속이 도입된 이리듐 촉매에서의 CO를 이용한 NOx 저감
Copyright Ⓒ 2020 KSAE / 174-01
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium provided the original work is properly cited.
Abstract
Nitrogen oxide(NOx) causes different types of environment pollution, including smog, acid rain, and fine particulate matter. Hence, NOx regulation has been continuously tightened because of the harmful effects of nitrogen oxide, as the necessity to develop de-NOx related technologies has emerged. In this study, we developed a catalyst that uses carbon monoxide(CO) as a reducing agent, instead of urea that is currently used in the NH3 selective catalytic reduction. Specifically, bimetallic catalysts were prepared through the co-impregnation of iridium and transition metals on alumina support. As a result, the Ir-Co catalyst showed more significant de-NOx performance than mere Ir and other Ir-based bimetallic catalysts. It was found that the highest de-NOx performance was obtained on an Ir-10 Co catalyst, where Co loading was 10 wt.%.
Keywords:
Selective catalytic reduction, NOx, de-NOx, Iridium catalyst, Bimetallic catalyst키워드:
선택적 촉매 환원, 질소산화물, 질소산화물 저감, 이리듐 촉매, 이종금속 촉매1. 서 론
자동차 배기가스에서 나오는 질소산화물(NOx)은 광화학적 스모그, 산성비를 일으키고 2차 미세먼지의 주요 원인물질로 알려져 있다. 이러한 유해성 때문에 유럽의 EURO 6, 미국의 Tier III 등과 같이 전세계적으로 질소산화물 규제를 만들어 배출량을 제한하고 있으며, 그 기준이 지속적으로 강화되고 있다. 기존 가솔린 엔진의 경우 질소산화물 저감을 위해 삼원촉매(Three way catalyst, TWC)가 많이 사용되었으나 디젤 엔진이나 린번(Lean-burn) 가솔린 엔진과 같이 과량의 산소가 배기가스에 함유된 조건에서는 질소산화물 저감에는 효과적이지 않다. 따라서 이를 대체할 배기가스 후처리 기술로 선택적 촉매 환원(Selective catalytic reduction, SCR)에 대해 많은 선행 연구가 이루어졌다. 선택적 촉매 환원은 촉매와 환원제를 사용하여 질소산화물을 선택적으로 환원시키는 기술을 말하며, 이때 환원제로 요소수(Urea), 탄화수소(HC), 수소(H2), 일산화탄소(CO) 등을 사용할 수 있다. 다양한 질소산화물 저감 기술 중에서 구리(Cu), 철(Fe)로 이온 교환된 제올라이트계 촉매와 요소수를 활용한 요소수 선택적 촉매 환원 기술(Urea-SCR)이 상용화 되어있다.1,2) 요소수 기반의 선택적 촉매 환원의 경우 질소산화물 저감효율 및 연비 향상의 효과가 우수하다는 장점이 있지만, 요소수나 암모니아를 저장 및 분사해주는 장치가 추가적으로 필요해 추가적인 비용이 발생하고, 배출가스 후처리 장치의 물리적인 부피가 커지게 되어 소형 경유차에 적용이 어렵다. 또한, 환원제로 작용하는 암모니아에 의한 Slipping 및 Fouling으로 인해 이차적인 오염이 발생할 수 있으며, 200 °C 이하 저온에서는 질소산화물 저감능력이 떨어지는 단점이 있다. 따라서 요소수 외 탄화수소, 수소, 일산화탄소 등 다른 환원제를 사용한 선택적 촉매 환원 기술에 대한 다양한 연구가 진행되었다. 에틸렌/프로필렌과 같은 불포화 탄화수소를 환원제로 사용하는 탄화수소 선택적 촉매 환원(HC-SCR)의 경우 비교적 양호한 질소산화물 저감능력을 보이지만 실제 엔진 운행조건에서는 저감능력 및 내구성이 떨어져 상용화 되지 못하고 있다. 환원제로 수소를 사용할 경우 200 °C 이하 저온 영역에서 높은 질소산화물 저감 능력을 보이며 배기가스 내에 이미 포함되어 있으므로 요소수 선택적 촉매 환원 장치와 달리 별도의 저장 및 분사 장치가 필요하지 않다. 따라서, 선택적 촉매 환원 장치 구축 비용이 절감되며, 소형 경유차량에도 도입이 가능하다. 또, 암모니아 환원제가 일으킬 있는 이차적인 환경오염으로 자유로워 친환경적이라는 장점이 있다. 하지만 많은 선행 연구들이 백금(Pt)과 팔라듐(Pd) 같은 귀금속 계열의 촉매로 이루어져 가격이 비싸며, 고온에서 재산화 및 소결 현상이 일어나 촉매 활성이 감소하는 단점을 갖고 있다. 환원제로 일산화탄소를 사용하게 되면 수소를 사용할 때와 마찬가지로 배기가스 내에 포함되어 있어 실제 선택적 촉매 환원장치 구축에 용이하며, 중온에서 비교적 안정적인 질소산화물 저감 능력을 가진 것으로 알려져 있다. 일산화탄소 선택적 촉매 환원(CO-SCR)의 경우 많은 선행연구들이 이리듐(Ir)기반 촉매들로 이루어져 있다.3-5)
Pt/SiO2에 WO3를 도입하거나, Ir/SiO2에 Nb2O5를 도입하는 등 SCR 반응에서 촉매 활성 높이기 위해 기존 촉매에 추가 성분을 도입하는 선행연구들이 보고되었다.6,7) 촉매에 금속 성분을 추가적으로 도입하여 이종금속 촉매를 제조할 수 있는데 이종금속 촉매는 그 두 금속 사이의 시너지 효과를 나타낸다고 알려져 있다.8) 그 예로, Ir-Pd/TiO2 이종금속 촉매의 경우 Ir/TiO2 촉매나 Pd/TiO2 촉매보다 높은 질소산화물 저감능력을 보인다고 보고된 바 있다.9)
본 연구는 기존 요소수(Urea) 대신 일산화탄소(CO)를 이용해 질소산화물을 저감하는 촉매, 구체적으로 기존 CO-SCR에 많이 쓰인 Ir/Al2O3 촉매에 전이금속을 함께 담지하여 기존보다 질소산화물 저감능력이 높은 촉매를 개발하기 위한 목적으로 연구를 진행하였다.
2. 실험 방법
2.1 촉매 제조
본 연구에서 사용된 이리듐 기반 이종금속 촉매는 다음과 같은 방법으로 제조하였다. 지지체로 상용 감마-알루미나(ɣ-Al2O3, SASOL, SBA-200), 이리듐의 전구체로는 염화이리듐(Ⅲ)수화물(IrCl3·xH2O, Alfa-Aesar, 99.8%), 전이금속 전구체로는 질산염 또는 아세트염 계열을 사용하였다. 이리듐과 전이금속 M의 전구체를 증류수에 교반을 통하여 용해시켰는데 이때 전구체의 양은 각각 지지체 ɣ-Al2O3 무게를 기준으로 이리듐의 담지량이 2 wt.%, 전이금속 M의 담지량은 1.5 wt.%와 10 wt.%가 되도록 하였다. 활성상 전구체가 증류수에 용해된 것을 확인한 뒤, 지지체 ɣ-Al2O3를 첨가하여 혼합한 후, 회전증발농축기를 통한 습윤함침법을 거쳐 담지를 진행하였다. 함침된 파우더 형태의 고체 생성물을 105 °C의 오븐에서 12 시간 동안 건조한 후, 공기 분위기에서 10 °C/분의 속도로 500 °C까지 온도를 올려준 뒤 동일온도에서 4 시간 동안 소성하였다. 제조된 촉매는 Ir-xM (M= Co, Fe, W, Zn, Mn, Cu, Mo) (x=1.5, 10)로 명명하였으며 여기서 x는 전이금속의 햠량(x wt.%)을 나타낸다. Ir과 Co 단독 담지 촉매와 역시 담지량을 각각 2 wt.%, 10 wt.%로 하여 위와 동일한 방법으로 제조하였다.
2.2 촉매 반응실험
2.1절에서 제조된 Ir 기반 담지 촉매들을 사용하여 CO-NO-O2 반응실험 통해 촉매의 질소산화물 저감 성능을 평가했다. 반응 가스의 조성은 50 ppm NO, 7000 ppm CO, 5 % O2, N2 balance로 설정하였고 150 ~ 350 °C의 온도 범위에서 25 ~ 50 °C 간격으로 반응을 진행하였다. 촉매양과 총유량은 각각 0.1 g, 200 ml/min으로 설정하였으며, 이때 사용하는 촉매는 압력 강하가 발생하는 것을 막기 위해 20 MPa의 압력으로 Palletizing 한 뒤 입자크기가 180 ~ 250 μm 되도록 해 반응기에 투입하였다. Ir 계열 촉매에서 활성상으로 사용되는 금속상의 Ir0을 만들어 주기 위해 10 %의 수소를 이용하여 450 °C에서 1시간 동안 환원전처리를 해주었다.10) 촉매들의 활성은 연속식 기상 반응기와 On-line으로 연결된 Gas cell FT-IR(Fourier Transform Infrared Spectroscopy)을 이용하여 가스 농도를 정성·정량적으로 측정하여 평가하였다. 질소산화물의 전환율을 이용하여 촉매의 질소산화저감 능력을 평가하였으며, 질소산화물의 전환율(NOx conversion), 일산화질소 전환율(NO conversion), 일산화탄소의 전환율(CO conversion)은 다음 식을 통하여 계산하였다.
| (1) |
| (2) |
| (3) |
| (4) |
2.3 촉매 특성분석
촉매 내 화학종들의 상태와 이들의 결정구조는 X-ray회절 분광법(XRD)을 이용하여 분석하였다. XRD 패턴은 X-ray 회절분석기(Smartlab, Rigaku)를 이용하여 40 kV and 30 mA에서 가속시킨 Cu-Kα 복사선을 촉매에 10 ~ 80 °범위에서 2.2 °/min 속도로 스캔하여 얻었다. 촉매의 환원적 특성을 알기 위해 H2-TPR분석을 실시하였다. H2-TPR분석은 BEL-CAT-II(BEL Japen Inc.)을 이용하여 석영관에 합성(소성)된 촉매 30 mg을 넣고 5 % H2/Ar을 30 ml/min 흘려주면서 상온에서 700 °C까지 10 °C/min의 속도로 온도를 올려주면서 변화하는 열전도도 검출기(Thermal conductivity detector, TCD) 신호를 측정하는 방식으로 이루어졌다.
3. 결과 및 토론
3.1 Ir-M 촉매 활성
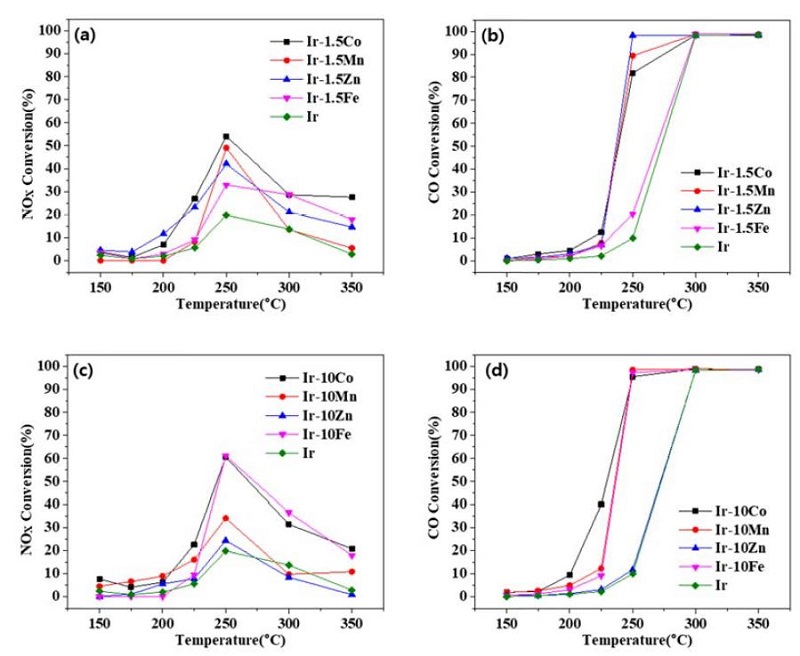
환원제로 CO를 활용한 Lean NOx reduction 반응을 수행했던 Ir-M 촉매들 중에서 준수한 NOx 전환율을 보였던 4종류의 Ir-M 촉매(M=Co, Ni, Fe, Mn)를 선정하여 전이금속 함량이 1.5 wt.%, 10 wt.%일 때 그리고 Ir 단독 담지 촉매의 각각의 온도에 따른 NOx 및 CO 전환율을 각각 Fig. 1에 도시하였다. Ir만 단독으로 담지한 촉매의 질소산화물 저감 능력은 온도가 올라갈수록 증가하여 250 °C에서 최대가 되며 이때 NOx 전환율은 약 20 %이다. 이후 온도가 더 높아지게 되면 NOx 전환율은 감소하게 되며 온도가 350 °C일 때의 NOx 전환율은 약 3 %로 떨어지게 된다. 이리듐과 전이금속 M 1.5 wt.%를 함침한 Ir-1.5M(M=Co, Ni, Fe, Mn) 촉매의 경우 200 °C 이하에서는 Ir-1.5Mn을 제외한 촉매들이 그 이후 온도 구간에서는 Ir-1.5Mn을 포함한 모든 촉매들의 질소산화물 저감능력이 증진됨을 알 수 있다. 질소산화물 저감 능력의 증진은 모든 촉매가 최고 저감능력을 갖는 250 °C에서 두드러지게 나타났다. Ir-1.5Co 촉매의 경우 250 °C에서의 NOx 전환율은 55 %이며, 이는 Ir 단독 담지 촉매의 NOx 전환율보다 2.5 배 이상 높고 다른 Ir-1.5M 촉매의 NOx 전환율(Ir-1.5Mn는 49 %, Ir-1.5Zn의 경우 42 %, Ir-1.5Fe의 경우 33 %)과 비교해도 높은 활성을 나타낸다. 이후 온도가 높아지면 Ir-1.5M 촉매는 Ir 단독 촉매와 마찬가지로 NOx 전환율이 감소하는 경향성을 보인다. Ir-M촉매에서 전이금속 M의 담지량을 10 wt.%로 증가시키면 250 °C에서 최고 활성을 가지며, 이보다 온도가 높아지게 되면 NOx 전환율이 점진적으로 감소하는 등 전체적인 경향성은 Ir-1.5M 촉매와 비슷하지만 각각의 다른 촉매마다 조금씩 다른 양상을 나타내게 된다. Ir-10Co 촉매의 경우 Ir-1.5Co 촉매와 마찬가지로 Ir-10M 촉매 중에서 250 °C에서 약 61 %로 가장 높은 활성을 나타냈다. Ir-10Mn 촉매는 200 °C 이하에서는 활성이 전혀 없던 Ir-1.5Mn와는 다르게 10 %이하로 작지만 질소산화물 저감능력을 나타냈다. 하지만 최고 활성을 나타내는 250 °C에서 Ir-10Mn 촉매의 NOx 전환율은 34 %로 49 %였던 Ir-1.5Mn 촉매에 비해 활성이 떨어졌다. Ir-10Zn 촉매는 모든 온도구간에서 Ir-1.5Zn 촉매보다 질소산화물 저감능력이 떨어졌다. Ir-10Fe 촉매는 Ir-1.5Fe 촉매와 달리 200 °C 이하의 온도에서는 활성을 나타내지 않지만, 그 이후부터 활성이 증가하기 시작해 250 °C에서의 NOx 전환율은 Ir-10Co와 동일한 61 %로 높은 NOx 전환율을 보였다. 하지만 200 °C 이하의 온도에서는 Ir-1.5Fe 촉매나 Ir-10Co 촉매와 비교하여 낮은 활성을 보였다.
환원제로 사용한 CO의 경우 NOx에 있는 산소원자나 반응가스 내 산소 분자와 반응하여 CO2로 전환된다. Ir 만 단독으로 담지한 촉매는 225 °C 이전까지는 CO 전환율이 3 % 이하로 낮고 300 °C 이후에는 100 % 가깝게 전환되는 Light-off curve를 따른다. Ir-M 촉매의 경우 Ir 단독 담지 촉매와 마찬가지로 Light-off curve를 따르며, 전이금속의 종류(Co, Mn, Zn, Fe) 및 함량(1.5 wt.%, 10 wt.%)과 상관없이 Ir 단독 담지 촉매에 비해 Light-off temperature가 저온으로 이동하는 사실을 알 수 있다. 구체적으로 전이금속 담지량이 1.5 wt.% 일 때 250 °C에서 Ir-1.5Zn, Ir-1.5Mn, Ir-1.5Co촉매는 각각 98 %, 89 %, 82 %의 CO 전환율을 보였으며, 담지량이 10 wt.% 일 때 Ir-10Co, Ir-10Mn, Ir-10Zn촉매는 250 °C 부근에서 Ir-10Zn 촉매의 경우는 300 °C에서 100 %에 가까운 CO 전환율을 보였다.
3.2 Ir-Co 촉매 활성
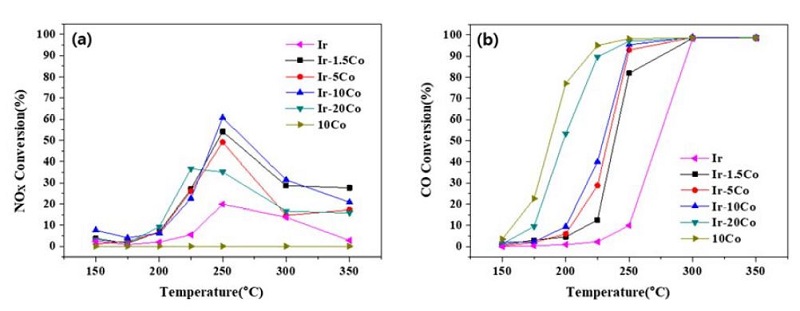
앞서 Ir-M 촉매 중에서 높은 활성을 보인 Ir-Co에 대하여 조성 최적화를 위해 Ir-Co 촉매에서 Co의 함량을 1.5, 5, 10, 20 wt.%로 변화시켜가며 반응 실험을 진행하였고, NOx, CO 전환율을 Ir, Co 단독 담지 촉매와 함께 Fig. 2에 도시하였다. 앞서 3.1 절에서 언급하였듯이 Ir 단독 담지 촉매의 경우 250 °C에서 약 20 %의 NOx 전환율을 갖지만, Co 만 단독으로 담지한 촉매의 경우는 모든 온도 구간에서 NOx 전환율이 0으로 활성이 없다. Co 함량에 상관없이 모든 Ir-Co촉매는 모든 온도구간에서 Ir 및 Co 단독 담지 촉매보다 높은 질소산화물 저감 능력을 가지며 250 °C에서 최대 NOx 전환율을 가진다. 구체적으로 Ir-10Co 촉매에서 61 %로 가장 크고 Ir-1.5Co 54 %, Ir-5Co 49 %, Ir-20Co 35 % 순으로 감소한다. 250 °C 이외의 대부분의 온도 구간에서도 Co가 10 wt.% 담지된 Ir-10Co 촉매가 높은 질소산화물 저감 능력을 나타낸다.
CO 전환율이 100 % 가까이 되는 온도인 Light-off temperature의 경우 Ir 단독 담지 촉매의 경우 Light-off temperature가 300 °C 부근인 반면 Co 단독 담지 촉매는 225 °C 부근으로 상대적으로 저온에 위치한다. Ir-Co 촉매에서의 Light-off temperature은 Co 함량이 1.5 wt.%에서 20 %로 높아질수록 300 °C에서 225 °C으로 저온으로 이동한다.
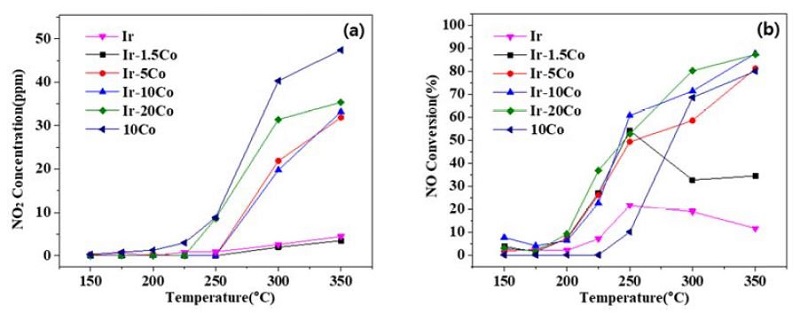
Co 함량 별 Ir-Co 촉매, Ir 단독 담지 촉매 그리고 Co 단독 담지 촉매의 NO2 농도와 NO 전환율을 Fig. 3에 도시하였다. Ir 단독 담지 촉매는 250 °C부터 소량의 NO2가 발생하기 시작하며 온도가 증가하면 발생량이 소폭 상승하지만 농도가 5 ppm을 넘지는 않았다. Ir-20Co촉매를 제외한 Ir-Co촉매 역시 250 °C부터 NO2가 발생하기 시작한다. Co 단독 담지 촉매의 경우 Ir 단독 담지 촉매나 Ir-Co 촉매와 비교하여 저온에서 NO2가 발생하기 시작하며 그 농도도 다른 촉매들보다 높았다. Co 함량이 높아짐에 따라 저온에서 환원제로 쓰인 CO 산화반응이 촉진되고 대부분의 CO가 소모되어 산화분위기인 반응조건에서 NO의 NO2로의 산화가 촉진된다. Ir-1.5Co촉매를 제외한 Ir-Co 촉매는 온도가 높아질수록 NO 전환율이 좋아졌으며 350 °C에서 Ir-5Co, Ir-10Co, Ir-20Co의 NO 전환율은 각각 81 %, 87 %, 87 % 였다. 이는 고온에서 NO가 NO2로 전환되기 때문에 NOx 전환율은 감소하지만 NO 전환율은 높아지는 것으로 나타났다.
3.3 Ir-Co 촉매 특성분석
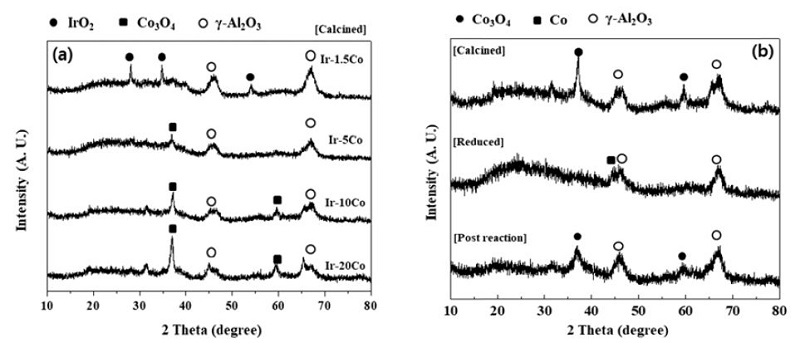
촉매 내 화학종들의 상태와 이들의 결정구조를 살펴보기 위하여 함량 별 Ir-Co 촉매를 소성 후 XRD 분석을 실시하여 Fig. 4(a)에 도시하였고, Ir-10Co 촉매를 소성 후, 환원전처리 후, 반응 후 3 종류의 상태에 대해 XRD 분석을 실시하여 Fig. 4(b)에 도시하였다. Fig. 4(a)를 살펴보면 모든 촉매에서 지지체로 쓰인 ɣ-Al2O3 피크가 나타났으며, Ir-1.5Co 촉매의 경우 28 °, 34.6 °, 54 °부근에서 IrO2 피크가 관찰되었지만 Co의 함량이 높아지면 관찰되지 않았다.11) 또한, Co 담지량이 5 wt.% 일 때부터 37 °와 65 °부근에서 Co3O4 피크가 관찰되기 시작하며 Co 함량이 증가함에 따라 Co3O4 피크가 크고 선명하게 나타남에 따라 상의 결정성이 증가함을 알 수 있다.12) Fig. 4(b)를 살펴보면 촉매 소성 후 선명하게 나타나던 Co3O4 피크는 환원전처리 과정을 거치면서 사라지는 것을 확인 할 수 있다. 사라졌던 Co3O4 피크는 반응 후 촉매에 다시 나타나게 되는데 이는 반응 과정에서 촉매의 재산화가 일어남을 알 수 있다.
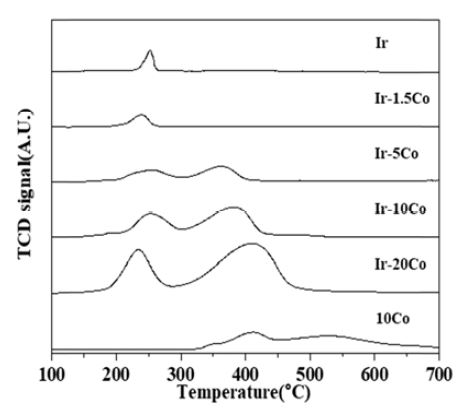
촉매의 환원 특성을 알아보기 위해 Ir-Co 촉매와 Ir 및 Co 단독 촉매를 H2-TPR(Tempeature Programmed Reduction) 분석을 시행하였고, 그 결과를 Fig. 5에 도시하였다. Ir 단독 촉매의 경우 240 °C 부근에서 환원 피크가 관찰되었으며 이는 IrO2가 금속 형태의 IrO로 환원되는 부분으로 알려져 있다.13) Co만 단독으로 담지한 촉매의 경우 2 개 경로를 걸쳐 환원이 된다고 알려져 있다. 저온에서 나오는 피크는 Co3O4가 CoO로 환원되는 피크이고, 상대적으로 고온에서 나오는 피크는 CoO가 금속형태의 CoO로 환원되는 피크이다.14) Ir-1.5Co 촉매의 경우 230 °C 부근에서 한 개의 환원 피크가 관찰되었으며, 나머지 Ir-Co 촉매들은 경우 2 개의 환원 피크가 관찰되었고, 모든 Ir-Co 촉매는 450 °C 이하에서 환원처리가 완료되었다. 이는 450 °C에서 10 %의 수소로 환원 전처리후 하는 과정이 합리적이며 전처리후 Co3O4 피크가 사라지는 XRD 결과 분석과도 일치한다. Ir-Co 촉매에서 Co 담지량이 늘어나면 첫번째 피크가 저온으로 이동하는데 이는 Ir과 Co의 이종금속 상호작용으로 촉매 환원성이 증진된 것으로 판단되며 비슷한 효과들이 다른 백금원소계(platinum group metal, PGM) 촉매에서 나타난다고 알려져 있다.15)
4. 결 론
2 차 미세먼지 발생의 주원인인 질소산화물(NOx)은 그 유해성 때문에 배출 규제가 지속적으로 강화되고 있으며, 관련기술 개발의 필요성이 제기되었다. 본 연구에서는 환원제로 기존에 쓰이던 요소수(Urea) 대신 일산화탄소(CO)를 사용하여 질소산화물을 줄이는 선택적 촉매 환원 촉매 개발을 수행하였다. 기존 CO-SCR 반응에 쓰이는 Ir 기반의 촉매에 다양한 종류의 전이금속을 함께 담지하여 이종금속 촉매를 제조하였다. 이종금속 촉매는 Ir 단독 담지 촉매와 비교하여 높은 질소산화물 저감 능력을 보였으며 특히 Ir-Co 촉매의 경우 Ir 단독 담지 촉매보다 2.5 배 이상의 높은 질소산화물 저감 성능을 보였다. 다양한 Co 함량의 Ir-Co 촉매에서는 Co 담지량이 10 wt.%일 때가 가장 높은 성능을 나타냈다. Ir-Co 촉매의 경우 고온에서 NO 전환율은 좋으나 다량의 NO2가 발생해 NOx 전환율이 감소하는 것에 착안해 추후 연구개발에 활용할 수 있을 것이다.
Acknowledgments
본 연구는 한국화학연구원에서 지원하는 SI1913-20(질소산화물 저감을 위한 요소수 무활용 신개념 촉매 원천기술 개발) 사업과 2020년 정부(과학기술정보통신부)의 재원으로 한국연구재단-기후변화대응기술개발사업의 지원을 받아 수행되었습니다(No. 2019M1A2A2103911). 서울대학교 공학연구원의 지원에도 감사드립니다.
References
-
J. Li, H. Chang, L. Ma, J. Hao and R. T. Yang, “Low-temperature Selective Catalytic Reduction of NOx with NH3 over Metal Oxide and Zeolite Catalysts-A Review,” Catalysis Today, Vol.175, Issue 1, pp.147-156, 2011.
[https://doi.org/10.1016/j.cattod.2011.03.034]

-
H. Hamada and M. Haneda, “A Review of Selective Catalytic Reduction of Nitrogen Oxides with Hydrogen and Carbon Monoxide,” Applied Catalysis A: General, Vols.421-422, pp.1-13, 2012.
[https://doi.org/10.1016/j.apcata.2012.02.005]

-
H. Inomata, M. Shimokawabe, A. Kuwana and M. Arai, “Selective Reduction of NO with CO in the Presence of O2 with Ir/WO3 Catalysts: Influence of Preparation Variables on the Catalytic Performance,” Applied Catalysis B: Environmental, Vol.84, Issues 3-4, pp.783-789, 2008.
[https://doi.org/10.1016/j.apcatb.2008.06.011]

-
M. Haneda, H. Kudo, Y. Nagao, T. Fujitani and H. Hamada, “Enhanced Activity of Ba-doped Ir/SiO2 Catalyst for NO Reduction with CO in the Presence of O2 and SO2,” Catalysis Communications, Vol.7, Issue 7, pp.423-426, 2006.
[https://doi.org/10.1016/j.catcom.2005.12.020]

-
T. Nanba, K. -I. Wada, S. Masukawa, J. Uchisawa and A. Obuchi, “Enhancement of Activity of Ir Catalysts for Selective Catalytic Reduction of NO with CO by Physical Mixing with SiO2,” Applied Catalysis A: General, Vol.380, Issues 1-2, pp.66-71, 2010.
[https://doi.org/10.1016/j.apcata.2010.03.028]

-
J. R. Regalbuto and E. E. Wolf, “An Integrated Study of Pt/WO3/SiO2 Catalysts for the NO/CO Reaction: III. FTIR Kinetic Study and Correlation of Promotional Effects,” Journal of Catalysis, Vol.109, Issue 1, pp.12-24, 1988.
[https://doi.org/10.1016/0021-9517(88)90180-7]

-
T. Tamai, M. Haneda, T. Fujitani and H. Hamada, “Promotive Effect of Nb2O5 on the Catalytic Activity of Ir/SiO2 for NO Reduction with CO under Oxygen-rich Conditions,” Catalysis Communications, Vol.8, Issue 6, pp.885-888, 2007.
[https://doi.org/10.1016/j.catcom.2006.09.004]

-
L. Liu, X. Guan, Z. Li, X. Zi, H. Dai and H. He, “Supported Bimetallic AuRh/ɣ-Al2O3 Nanocatalyst for the Selective Catalytic Reduction of NO by Propylene,” Applied Catalysis B: Environmental, Vol.90, Issues 1-2, pp.1-9, 2009.
[https://doi.org/10.1016/j.apcatb.2009.02.022]

-
J. Li, G. Wu, N. Guan and L. Li, “NO Selective Reduction by Hydrogen over Bimetallic Pd-Ir/TiO2 Catalyst,” Catalysis Communications, Vol.24, pp.38-43, 2012.
[https://doi.org/10.1016/j.catcom.2012.03.014]

-
K. Ueda, M. Yoshida, K. Isegawa, N. Shirahata, K. Amemiya, K. Mase, B. S. Mun and H. Kondoh, “Operando Observation of NO Reduction by CO on Ir(111) Surface Using NAP-XPS and Mass Spectrometry: Dominant Reaction Pathway to N2 Formation under Near Realistic Conditions,” The Journal of Physical Chemistry C, Vol.121, No.3 pp.1763-1769, 2017.
[https://doi.org/10.1021/acs.jpcc.6b11583]

-
P. C. Liao, C. S. Chen, W. S. Ho, Y. S. Huang and K. K. Tiong, “Characterization of IrO2 Thin Films by Raman Spectroscopy,” Thin Solid Films, Vol.301, Issues 1-2, pp.7-11, 1997.
[https://doi.org/10.1016/S0040-6090(96)09545-4]

-
C. -S. Cheng, M. Serizawa, H. Sakata and T. Hirayama, “Electrical Conductivity of Co3O4 Films Prepared by Chemical Vapour Deposition,” Materials Chemistry and Physics, Vol.53, Issue 3, pp.225-230, 1998.
[https://doi.org/10.1016/S0254-0584(98)00044-3]

-
E. Pachatouridou, E. Papista, A. Delimitis, M. A. Vasiliades, A. M. Efstathiou, M. D. Amiridis, O. S. Alexeev, D. Bloom, G. E. Marnellos, M. Konsolakis and E. Iliopoulou, “N2O Decomposition over Ceriapromoted Ir/Al2O3 Catalysts: The Role of Ceria,” Applied Catalysis B: Environmental, Vol.187, pp.259-268, 2016.
[https://doi.org/10.1016/j.apcatb.2016.01.049]

-
X. Hu, D. Dong, X. Shao, L. Zhang and G. Lu, “Steam Reforming of Acetic Acid over Cobalt Catalysts: Effects of Zr, Mg and K Addition,” International Journal of Hydrogen Energy, Vol. 42, Issue 8, pp.4793-4803, 2017.
[https://doi.org/10.1016/j.ijhydene.2016.12.033]

-
R. Zhu, Q. Yan, J. He, G. Cao and F. Ouyang, “Simultaneous Removal of Soot and NOx with Ru-Ir/TiO2 Catalyst under Oxygen-rich Condition,” Applied Catalysis A: General, Vol.541, pp.42-49, 2017.
[https://doi.org/10.1016/j.apcata.2017.04.014]